La radioactivité
Si on observe un noyau, il finira par se désintégrer.
Mais on peut attendre parfois longtemps, et ce temps d'attente est imprédictible.
Par contre, statistiquement sur un grand nombre de noyau, ce temps suit une loi bien connue, caractérisée par ce qu'on appelle la demi-vie.
Si on prend une certaine quantité d'atomes radioactifs, on constate que
- le nombre de désintégrations est proportionnel à la quantité d'atomes
- le nombre de désintégrations est proportionnel au temps
ce qui mène à une loi exponentielle :
λ est la constante de désintégration.
On aime mieux utiliser comme paramètre ce qu'on appelle la demi-vie : c'est le temps qu'il faut pour que la moitié des atomes initiaux se désintègrent. La demi-vie caractérise entièrement la courbe :
C'est une distribution binomiale, et pour un grand nombre d'atomes (N≫1) et une courte durée (∆t≪1), ça suit une loi de Poisson.
Il existe des études pour voir de possibles déviations dans des cas extrêmes, sans succès. La loi est très bien vérifiée.
Quelques demi-vies
La demi-vie est constante pour un élément donné, elle ne varie jamais, par contre on observe des disparités importantes entre les éléments.
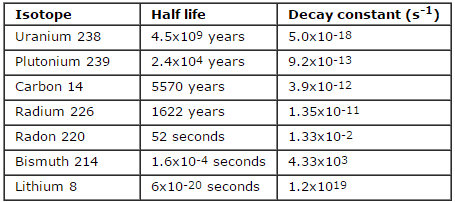
La demi-vie est plus parlante que la constante !
Datation au carbone 14
Le carbone 14 est produit régulièrement en haute atmosphère lors de réactions nucléaires induites par des neutrons rapides d’origine stellaire.
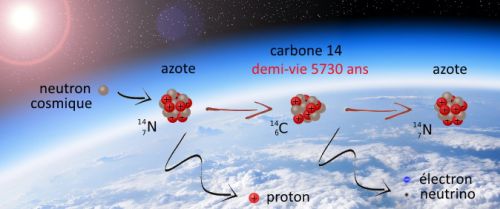
Il est en proportion à peu près constante dans les environnements terrestres :
Lorsqu’un individu ou une plante meurt, son métabolisme cesse de fonctionner, son carbone n’est plus renouvelé et le carbone 14 qu’il contient se désintègre en redonnant un noyau d’azote 14 avec une demi-vie de 5730 ans.
Il suffit alors de mesurer la proportion du carbone 14 dans les restes pour connaître l’époque de la mort.
Le tableau de stabilité
Existe-t-il une règle pour savoir si un isotope sera plus stable qu'un autre ?
Eh bien pas vraiment, comme on peut le constater sur ce qu'on appelle le tableau de stabilité des noyaux atomiques.
On met sur un axe le numéro atomique (le nombre de protons) et sur l'autre axe le nombre de neutrons (les isotopes à nombre de protons égal), et on donne un code couleur pour indiquer la demi-vie.
C'est assez étrange, à bien y regarder. Il existe des tentatives de modélisation, mais bon, avec une structure pareille, il doit falloir se lever de bonne heure.
C'est une vision très résumée, on trouvera plus de détails ici : Stabilité et instabilité des noyaux atomiques par Elucid
Heureusement pour nous, mais c'est un peu normal sinon on ne serait pas là, la plupart des atomes de notre corps sont suffisamment stables. Ouf.
Mais n'oublions pas que nous avons vraiment beaucoup d'atomes dans un corps, et que même des demi-vies élevées n'excluent pas d'avoir des désintégrations, d'ailleurs on vient de voir le cas du carbone 14.
Et quels effets ces rayonnements produisent sur le vivant ?